Op 5 juli lanceerde Novo Nordisk een fase III klinische proef met CagriSema-injectie in China, met als doel de veiligheid en werkzaamheid van CagriSema-injectie te vergelijken met semeglutide bij patiënten met obesitas en overgewicht in China.
CagriSema-injectie is een langwerkende combinatietherapie die wordt ontwikkeld door Novo Nordisk. De belangrijkste componenten zijn GLP-1 (glucagon-like peptide-1) receptoragonist smeglutide en een langwerkende amyline-analoog cagrilintide.CagriSema-injectie kan eenmaal per week subcutaan worden toegediend.
Het primaire doel was om CagriSema (2,4 mg/2,4 mg) te vergelijken met semeglutide of placebo eenmaal per week subcutaan.Novo Nordisk heeft de resultaten bekendgemaakt van een proef met CagriSema voor de behandeling van stadium 2-diabetes, waaruit bleek dat het hypoglycemische effect van CagriSema beter is dan dat van semeglutide, en dat bijna 90% van de proefpersonen het HbA1c-doel heeft bereikt.
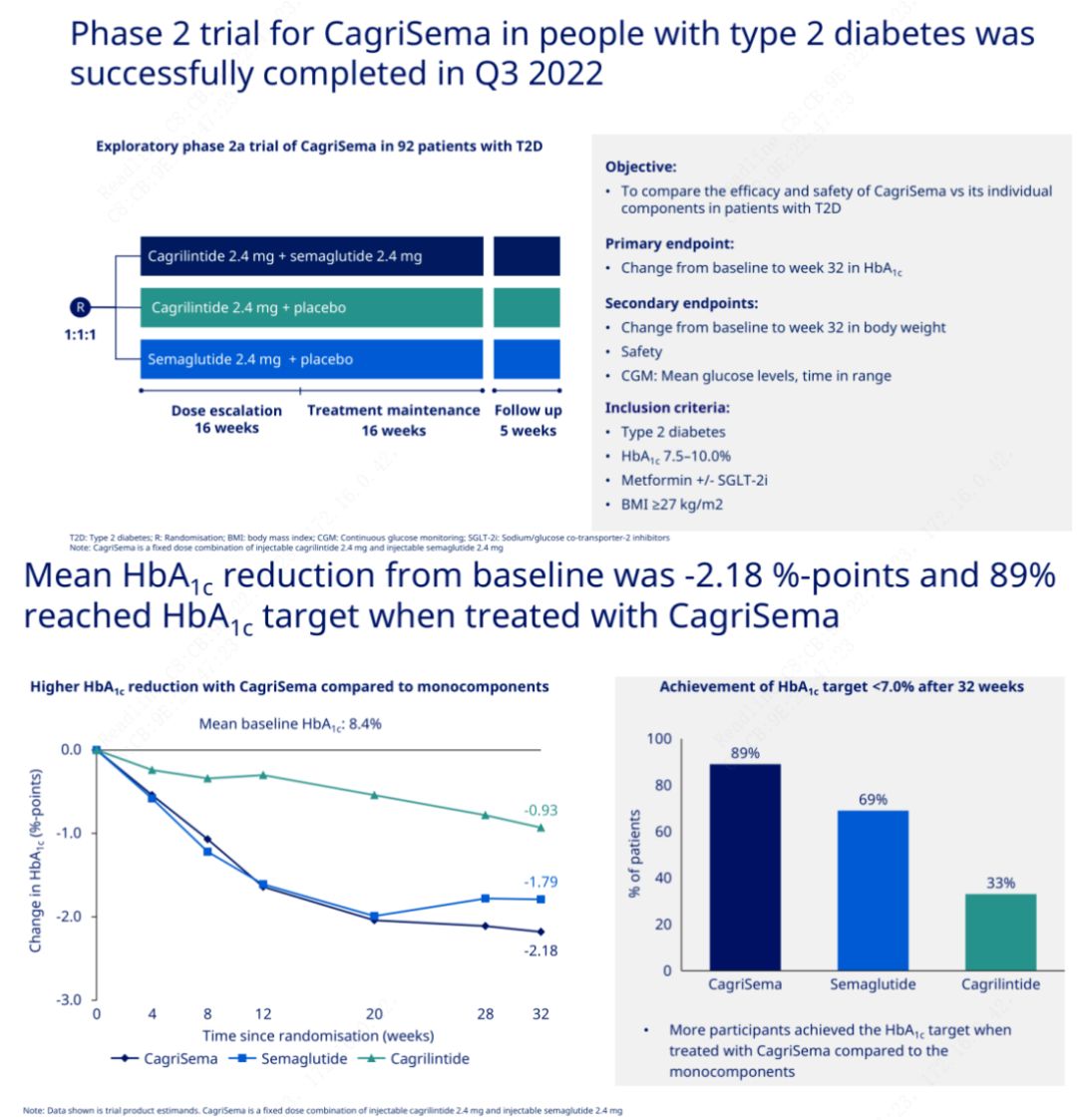
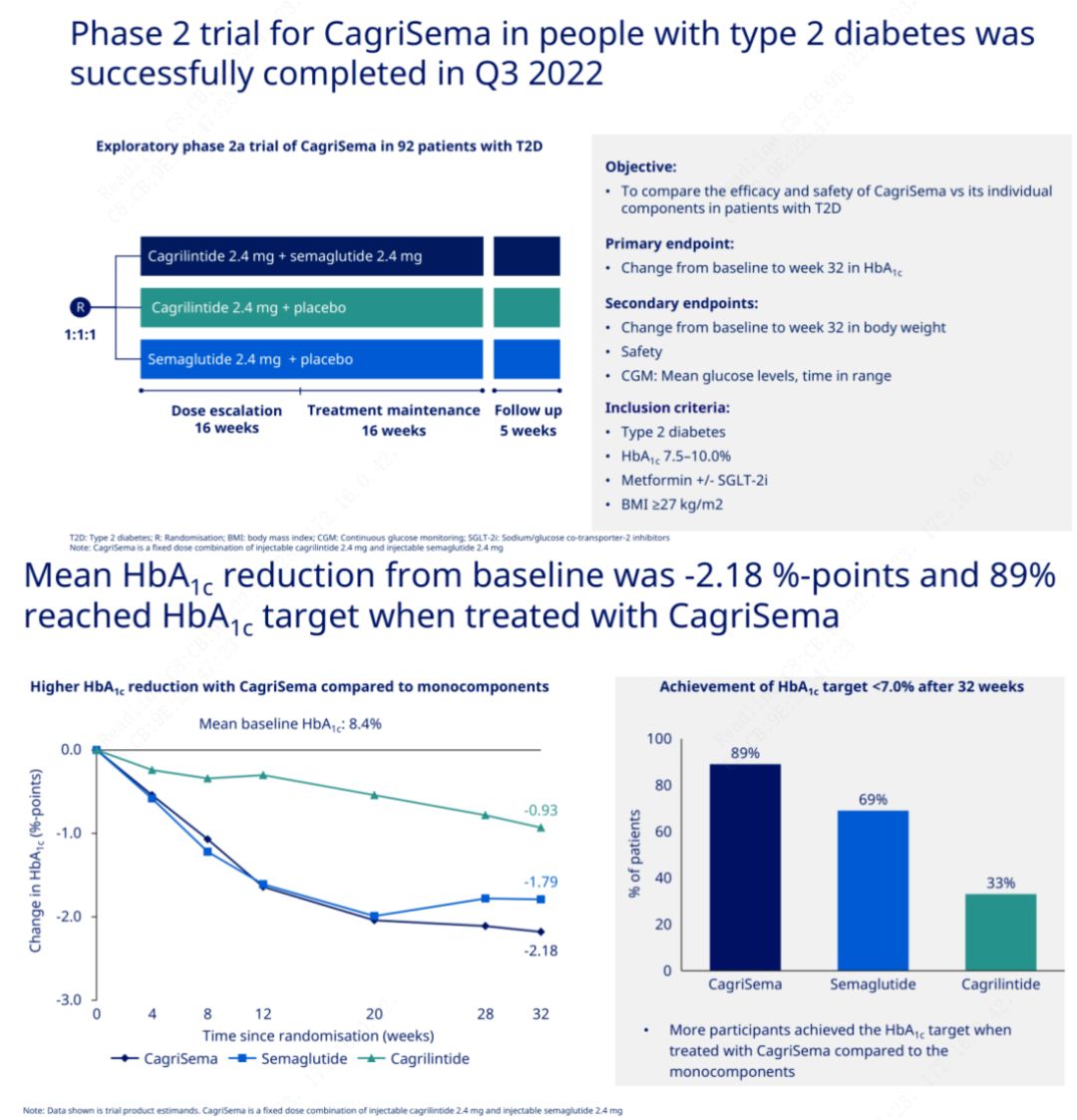
Uit de gegevens bleek dat, naast het significante hypoglykemische effect, in termen van gewichtsverlies, CagriSema-injectie significant beter presteerde dan semeglutide (5,1%) en cagrilintide (8,1%), met een gewichtsverlies van 15,6%.
Het innovatieve medicijn Tirzepatide is 's werelds eerste goedgekeurde wekelijkse GIP/GLP-1-receptoragonist.Het combineert de effecten van twee incretines in één enkel molecuul dat één keer per week wordt geïnjecteerd en is een nieuwe klasse behandelingen voor type 2-diabetes.Tirzepatide werd in mei 2022 goedgekeurd door de Amerikaanse Food and Drug Administration (FDA) om de glykemische controle (op basis van voeding en lichaamsbeweging) bij volwassenen met diabetes type 2 te verbeteren en is momenteel goedgekeurd in de Europese Unie, Japan en andere landen.
Op 5 juli kondigde Eli Lilly een fase III SURPASS-CN-MONO-onderzoek aan naar het platform voor registratie van klinische geneesmiddelenonderzoeken en het vrijgeven van informatie voor de behandeling van type 2-diabetespatiënten.SURPASS-CN-MONO is een gerandomiseerde, dubbelblinde, placebogecontroleerde fase III-studie, ontworpen om de werkzaamheid en veiligheid van tirzepatide-monotherapie te evalueren in vergelijking met placebo bij mensen met type 2-diabetes.Het was de bedoeling om 200 patiënten met type 2-diabetes te includeren die in de 90 dagen voorafgaand aan bezoek 1 geen antidiabetica gebruikten (behalve in bepaalde klinische situaties, zoals acute ziekte, ziekenhuisopname of electieve operatie, kortdurend (≤14 dagen) gebruik van insuline).
Type 2-diabetes zal naar verwachting dit jaar worden goedgekeurd
Vorige maand werden de resultaten van een SURPASS-AP-Combo-studie op 25 mei gepubliceerd in het blockbuster-tijdschrift Nature Medicine.De resultaten toonden aan dat Tirzepatide vergeleken met insuline glargine een betere HbA1c- en gewichtsreductie liet zien in de populatie van type 2-diabetespatiënten in de regio Azië-Pacific (voornamelijk China): HbA1c-reductie tot 2,49% en gewichtsreductie tot 7,2 kg (9,4%) na 40 weken behandeling waren de significante verbetering van de bloedlipiden en bloeddruk, en de algehele veiligheid en verdraagbaarheid goed.
De klinische fase 3-studie van SURPASS-AP-Combo is de eerste studie van Tirzepatide die voornamelijk wordt uitgevoerd bij Chinese patiënten met type 2-diabetes, onder leiding van professor Ji Linong van het Peking University People's Hospital.SURPASS-AP-Combo komt overeen met de resultaten van de wereldwijde SURPASS-onderzoeksreeks, die verder bewijst dat de pathofysiologie van diabetes bij Chinese patiënten consistent is met die van mondiale patiënten, wat de basis vormt voor het gelijktijdige onderzoek en de ontwikkeling van nieuwe medicijnen in China en de wereld, en biedt ook solide bewijsondersteuning om Chinese patiënten de kans te geven de nieuwste medicijnen voor de behandeling van diabetes en hun klinische toepassing zo snel mogelijk in China te gebruiken.
Posttijd: 18 september 2023

